pH值的计算
pH值的计算pHzhi de jisuan
常用H+浓度来表示溶液的酸碱性,当[H+]小于1mol·L-1时,为了使用方便,常用氢离子的负对数,即-1g[H+]来表示溶液的酸度,并称为pH值,即pH=-1g〔H+〕。
任何物质的水溶液中[H+]·[OH-]=Kw,室温时Kw=1×10-14。纯水中[H+]=[OH-]=10-7mol·L-1,则 pH=-1g[H+]=7。在其他中性溶液中[H+]=[OH-]=10-7mol·L-1,pH也为7;酸性溶液中[H+]>[OH-],其pH<7;碱性溶液中[H+]<[OH-],其 pH>7。氢氧离子浓度的负对数也可表示为pOH,则溶液的pH+pOH=14,pH=14-pOH。计算溶液的pH值关键在于正确求出各种溶液的[H+],具体计算如下:
例1 计算0.01mol·L-1盐酸溶液的pH值。解 盐酸是强电解质,在水中全部电离
[H+]=0.01mol·L-1 pH=-1g[H+]=-1g 0.01=2
答 该溶液的pH为2。
例2 计算c=0.1mol·L-1醋酸溶液(电离度α=1.34%)的pH值。
解 醋酸是弱电解质在水中部分电离
[H+]=α·c=1.34%×0.1
=1.34×10-3(mol·L-1)
pH=-1g[H+]=-1g1.34×10-3=2.87答 该溶液的pH为2.87。
例3 计算c(NaOH)=0.1mol·L-1氢氧化钠溶液的pH值。
解 NaOH为强电解质在水中全部电离[OH-]=0.1mol·L-1
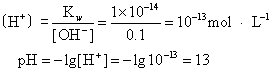
另一算法:
pH=14-pOH=14-(-1g[OH-])=14-1=13答 该氢氧化钠溶液的pH为13。
例4 某溶液的pH=5求该溶液的H+和OH-的浓度。
解 pH=5=-1g [H+]
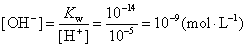
答 该溶液的H+浓度为10-5mol/L,OH-浓度为10-9mol/L。
☚ 十字交叉法 溶液稀释后的pH值计算 ☛
- 如何理解车间(分厂)民主管理?是什么意思
- 如何理解车间民主管理小组?是什么意思
- 如何理解车间民主管理的日常活动?是什么意思
- 如何理解车间民主管理的组织制度?是什么意思
- 如何理解车间职工大会?是什么意思
- 如何理解集体企业厂长(经理)对职工(代表)大会负责?是什么意思
- 如何理解集体企业厂长(经理)提出召开职工(代表)大会的建议?是什么意思
- 如何理解集体企业的职工(代表)大会?是什么意思
- 如何理解集体企业职工代表大会代表?是什么意思
- 如何理解集体所有制企业的民主管理?是什么意思
- 如何申请再审?是什么意思
- 如何申请我国法院承认和执行外国的裁判?是什么意思
- 如何申请撤诉?撤诉后能再起诉吗?是什么意思
- 如何看准股票买卖时机?是什么意思
- 如何看待企业经营者收入高于职工收入现象?是什么意思
- 如何看待近两年来性病报告数出现下降是什么意思
- 如何看汤色是什么意思
- 如何确定企业工资总额与经济效益挂钩的浮动比例?是什么意思
- 如何确定和处理无效集体合同?是什么意思
- 如何确定商品采购成本?是什么意思
- 如何确定商品采购的入帐时间?是什么意思
- 如何确定商品销售的入帐价格?是什么意思
- 如何确定固定资产的原始价值?是什么意思
- 如何确定房地产开发企业的成本核算对象?是什么意思
- 如何确定房地产开发企业的成本项目?是什么意思
- 如何确定施工企业大堆材料的耗用量?是什么意思
- 如何确定施工企业未完施工和已完工程成本?是什么意思
- 如何确定旧资产的现行成本?是什么意思
- 如何确定被告所在地?只能向被告所在地的法院起诉吗?是什么意思
- 如何确定设计方案与工程概算是什么意思
- 如何确定适当的承包期限?是什么意思
- 如何移交与调阅出纳归档资料?是什么意思
- 如何签订专利许可证合同?是什么意思
- 如何管理药品广告?是什么意思
- 如何管理药品的生产?是什么意思
- 如何管理药品的进、出口?是什么意思
- 如何管理银行账户?是什么意思
- 如何组织好职工讲演活动?是什么意思
- 如何组织施工企业内部往来的核算?是什么意思
- 如何织纨素,自着蓝缕衣是什么意思
- 如何结转本年利润?是什么意思
- 如何结转股份制企业的全年利润?是什么意思
- 如何维护工会积极分子的正当权益?是什么意思
- 如何编制出纳报告?是什么意思
- 如何编制损益表?是什么意思
- 如何编制施工企业会计报表?是什么意思
- 如何编制现行成本财务报表?是什么意思
- 如何编制现金收款记账凭证?是什么意思
- 如何编制股份制企业的资产负债表?是什么意思
- 如何编制财务状况变动表?是什么意思
- 如何落实民主评议?是什么意思
- 如何装订与保管会计凭证?是什么意思
- 如何观察结肠造口是什么意思
- 如何解决奥林匹克知识产权侵权纠纷?是什么意思
- 如何解决租赁经营合同双方发生的纠纷?是什么意思
- 如何解决集体合同纠纷?是什么意思
- 如何计征个人收入调节税?是什么意思
- 如何计提和核算存货变现损失准备?是什么意思
- 如何计算企业在货币性项目净额上的购买力损益?是什么意思
- 如何计算债券的发行价格?是什么意思